

| 国立研究開発法人日本医療研究開発機構(AMED:Japan Agency for Medical Research and Development)の発足から1年が経過したことから、今回は、末松誠AMED理事長を迎え、同機構発足の経緯や現状の活動について紹介して頂くとともに、臨床医が医学研究に果たす役割や、あるべき医療研究の姿について、横倉会長と語り合って頂いた。 |
|---|
横倉 AMEDが発足して1年が経ちましたが、改めて発足の経緯についてご紹介頂けますか。
末松 日本では、医療研究開発の競争的資金が年間およそ1400億円あり、それ以外に文部科学省の科学研究費助成事業(科研費)とか、ナショナルセンター(国立高度専門医療研究センター)の経常費的なものもあります。医療研究開発の競争的資金については文科省、厚生労働省、経済産業省の三つの資金が、それぞれのルールで細分化して配分されていましたが、これを健康・医療戦略推進本部の強力なイニシアチブで1カ所に統合し、一元管理することで全体的に最適化できないかという発想で設立されたのがAMEDです。一元管理によって、医療研究開発の成果を患者さんに少しでも早く還元することができればと思っています。
横倉 三つの省から、資金だけでなく人も来られている訳で、ご苦労も多いのではないかと思いますが、その辺りは、いかがでしょうか。
末松 それぞれの省の省益もあり、お互いに引っ張り合うのではなど、ご心配下さる方もいたのですが、思いのほか三者は協力的でした。
実は、三つの役所は違うルールの下で医療研究開発の資金を配分していましたので、例えて言えば、一つのグラウンドでサッカーと野球とラグビーを同時にやっているような状態でした。それが昨年の4月に一緒になった訳ですから、発足当初、研究者の方々には大変ご迷惑をかけたと思います。
しかし、この三省から来られた方々が協力的でしたし、司令塔として内閣官房の他に財務省からも加わってもらい、研究費を非常に円滑かつ機動的に運用するルールに統一することができました。ただ、研究機関や研究しながら診療に携わっている一般の先生方に広く浸透するには、もう少し時間がかかると思いますが、ルールを1年以内に変更できたことは、大きな成果だと思っています。
横倉 それは良かったですね。見込みのある研究とか日本の将来を考えた研究などの分野に重点的に資金を投入し、研究体制をつくっていくことができるということなのでしょうね。
末松 実は、昨年の4月は現存するプロジェクトの金額そのままでAMEDの予算の骨格がつくられていました。今、その一つひとつに関して、金額が領域に合っているか、お金の運用ルールが基になって研究がやりにくくなっていないかを徹底的にチェックし、研究体制の更なる最適化を進めているところです。
AMEDの予算は、国民の皆さんの税金で成り立っていますので、もし大きな経済のクライシスが起きても慌てずに済むように、例えばジカ熱やエボラ出血熱など、時々刻々と変化する世界の動向や情報を集めながら弾力的に運用する部分と、難病の患者さんやご家族といった医療弱者への支援など、簡単に減らしてはいけない部分とに分けて、機動的に運用すべきところは運用できるよう、今後もっとメリハリをつけていこうと考えていますが、まだ道半ばと言ったところです。
横倉 楽しみですね。
「未診断疾患イニシアチブ診断体制」とは
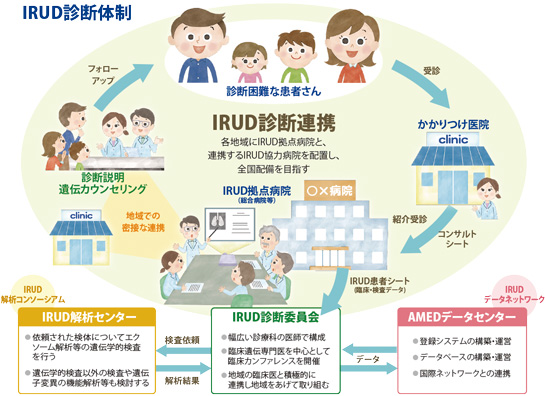 横倉 AMEDの最近の活動として、日常の臨床現場で診断がつかない希少疾患等の患者さんの診断を確定して病態を解明しようとする取り組みで、「未診断疾患イニシアチブ(IRUD:Initiative on Rare and Undiagnosed Diseases)診断体制」の構築がありますね。
横倉 AMEDの最近の活動として、日常の臨床現場で診断がつかない希少疾患等の患者さんの診断を確定して病態を解明しようとする取り組みで、「未診断疾患イニシアチブ(IRUD:Initiative on Rare and Undiagnosed Diseases)診断体制」の構築がありますね。
末松 ご存知のように、希少疾患や未診断疾患、特に何万人に一人という確率でしか発症しないような疾患の場合には、かかりつけ医がその異変に気付いて、地域の中核病院の専門医に相談をする、それでも似たような患者さんを診たことがないため、診断がつかないということが多くあります。それは大学病院に行っても同じで、いくら血液を調べても、よく似た病気は教科書に載っているけれども、「ちょっと違うな」という症例が、一番診断が難しい訳です。それで、別の大学病院に行き、最後にナショナルセンターに行っても診断がつかない。
そのような場合、根本的な解決はできないけれども、地域の中核病院や開業医の先生方の多くは、患者さんの精神的苦痛やご家族の負担を取り除き、安心を提供できないかと闘っておられるはずなのです。
そこで、AMEDでは、日常の臨床現場で診断がつかない希少疾患等の患者さんの診断を確定し、病態の解明を進めるためにIRUDの構築と研究を進めています。これは、かかりつけ医とIRUDに参加する拠点病院の医師が連携し、希少疾患に詳しい専門家の知見及び最先端の遺伝子解析等を用いた検査結果を総合して診断を確定しようというものです。これらの研究を推進することで、将来的には、希少・未診断疾患の診断基準の普及や体系的な治療等に結び付くことを期待しています。
AMEDでは、まず東京都をモデル地区として、未診断疾患患者の実態把握のための調査を実施しようと考え、昨年、横倉会長にご協力頂けないかということでお伺いした次第です。
横倉 あれは1年くらい前でしたかね。私どもも協力できればと思い、昨年11月には東京都医師会に実態調査への協力を依頼したところです。
今年の1月には、NIH(National Institutes of Health:米国国立衛生研究所)と研究協力に関する覚書を締結されたそうですが、その取り組みと今後の見通しについても教えて頂けますか。
末松 NIHのUDP(Undiagnosed Diseases Program:未診断患者プロジェクト)の過去8年間の累計では、子どもが4割、大人が6割ですが、ゲノム解析という方法を使って、かかりつけ医あるいは地域の中核病院の主治医とNIHの先生がやりとりをした結果、新しい疾患概念と分かった症例が数十例出てきて、人種を越えて情報を共有すれば、もっと早く見つかる可能性があるのではないかというニーズがあることが分かりました。
幸い日本は、国民皆保険であり、厚生省時代には難病対策の法律が制定されるなど、診療と研究を法律に基づいて支える仕組みがあったため、医師の難病に対する経験値は、世界的にも非常に高いレベルにあります。
日米、日英、あるいはアジアの国同士で、患者さんの情報を共有し、症状を見て、この患者さんと自分の診ている患者さんとは同じ疾患ではないかと分かるような仕組みがあってもよいのではないかということが私の大きなモチベーションになって、NIHと協定を結ぶことになりました。
この協定は、難病だけではなく、新しく出てきた多剤耐性菌やウイルスといった感染症も対象としており、国境を越えてデータを共有することによって、課題が一気に解決できるのではないかと考えています。
横倉 非常に期待される取り組みですね。実は、3月20日に日医会館で、日本獣医師会との共催により、"One Health"ということで、「人獣共通感染症と薬剤耐性」というテーマのシンポジウムを開催したのですが、その中でも、現在使われている抗生剤の7割が動物に使われているという話がありました。
末松 すごい量が使われているのですね。
横倉 そのことによって耐性菌が相当出ているようです。
末松 幸いなことにわが国は、国立感染症研究所と農林水産省の間の情報共有が比較的うまくいっていますし、カナダやオーストラリアなど、家畜の数の方が人間より多いところでも、農業系の微生物の情報と人間の耐性菌に関する情報の共有化が進んでいると聞いていますし、今後この分野での研究も進むと思っています。
横倉 いわゆる"かかりつけ医"である会員の先生方にも非常にお困りの患者さんがおられると思うので、ぜひIRUDで、それらの解明につなげて頂ければと思います。
医学研究における臨床医の役割
 末松 私は特に日医会員の先生方に大変期待をしているのです。ゲノム研究者の中には、患者さんからゲノムサンプルを集めて、次世代シークエンサー(第2世代シークエンサーとも呼ばれ、ランダムに切断された数千万のDNA断片の塩基配列を同時並行的に決定することができる)で解析すれば全部診断がつくと誤解している人がいるかも知れません。しかし、遺伝子疾患の診断で大事なのはゲノム解析ではなく、実際に患者さんを診て、表面的に現れてくる症状とか血液中の異常などを拾い上げることであり、それを行っているのは一般の臨床の先生なのです。いくつかの症状・症候が一致している人を2人診た、あるいは3人診た時に初めて、その人達のゲノムを調べようとなるのであって、ゲノムの基礎研究者の考え方では、きちんとした診療はできません。
末松 私は特に日医会員の先生方に大変期待をしているのです。ゲノム研究者の中には、患者さんからゲノムサンプルを集めて、次世代シークエンサー(第2世代シークエンサーとも呼ばれ、ランダムに切断された数千万のDNA断片の塩基配列を同時並行的に決定することができる)で解析すれば全部診断がつくと誤解している人がいるかも知れません。しかし、遺伝子疾患の診断で大事なのはゲノム解析ではなく、実際に患者さんを診て、表面的に現れてくる症状とか血液中の異常などを拾い上げることであり、それを行っているのは一般の臨床の先生なのです。いくつかの症状・症候が一致している人を2人診た、あるいは3人診た時に初めて、その人達のゲノムを調べようとなるのであって、ゲノムの基礎研究者の考え方では、きちんとした診療はできません。
何歳ぐらいの時にどういう症状が出たか等、カルテの記録全てが貴重な情報になる訳で、症状などをきちんと正確に記載することが、いかに大変かつ重要なことかを一番ご存知なのは日々診療をされている医師会の先生方のはずです。ですから、IRUDの話を最初に横倉会長に聞いて頂きたくて、1年前にその話をしにきたのです。
横倉 地域で一生懸命頑張っている先生方には、医師として、通常の診療のみならず、医学研究者としての気持ちも常に持って欲しいということですね。
末松 ええ、そういう気持ちを持って頂きたいと思います。一方で研究者の人達は、もちろん論文が『Nature』とか『Nature Genetics』『Cell』などに掲載されることは良いことなのですが、その論文の紙を患者さんが食べても病気が治る訳ではないということを自覚するべきです。臨床医と研究者が両方からトンネルを掘っていくことで助かるのは患者さんですから、ぜひ形にしていきたいと思っています。
横倉 実は、日医でも、医師主導治験のモデル研究の実施やさまざまな啓発活動を通じて、わが国の治験実施基盤の整備を進める「臨床研究・治験推進研究事業」を平成15年から実施しています。更に、昨年6月からは、広く臨床医が医療機器の開発や事業化を進める窓口を提供し支援を行うことで、新たな医療機器や技術の開発を促進し、国民により高い治療技術を提供していくことを目的として、「医師主導による医療機器の開発・事業化支援事業」をスタートさせました。診断よりは治療面のアイデアが多いようですが、既に90数種類に及ぶアイデアが全国の先生方から寄せられており、ぜひその中から一つでも大きな貢献ができるようなものがつくれたらと思っています。
末松 薬の場合にはまず化合物ありきで、それが疾患標的分子をどう制御するかという話から開発が進む訳ですが、特に、医療機器の開発は薬とは全く逆で、何と言っても医療現場にいる先生が、どういう医療機器が欲しいかということを最もよく知っておられる訳です。
医療行為はアートの領域にあると言われる中で、ちょっとした工夫や器具によって、誰でも同じような結果が得られるようになれば、大きな福音になりますから、先生達の発想の中から、実際に広く使われるような医療機器が必ず出てくるだろうと、大変期待しています。
横倉 その他にも、「診療所向けの糖尿病疾病管理データベース」の構築も現在検討中です。専門医にかかる前の状態等を把握することで、できるだけ合併症を起こさないような管理につなげていければと考え、取り組んでおります。
末松 実はIRUDでもそういうデータベースを構築するプランがあります。未診断疾患の患者さんの複数の症状・表現型の組み合わせをデータベース化しておき、国内、更には国外の同じような症状の組み合わせの患者さんを探せるようにしたいと考えています。
現にIRUDの企画に興味を持って頂いた臨床医の先生が、IRUDの紹介をするシンポジウムにたまたま参加して下さり、何年も診断が確定しなかった患者さんが偶然2名おられ、主治医の先生及び患者さんの同意の下にエクソーム解析(全ゲノムのうち、エクソン配列のみを網羅的に解析する方法)を行い、同一の遺伝子の異常であることが証明され、新しい疾患概念として認められたケースが早くも出てきました。
現在は、これが論文化され、同じような未診断の患者さんをもたれている主治医の方々から国境を越えて問い合わせがくるようになりつつあります。
治療に展開することが今後の課題ですが、きちんと理由があって病気になられているということがはっきりすることは医療の重要な使命の一つと考えます。
いろいろ技術的な問題や、ゲノム編集という画期的な技術も危険な部分は当然ある訳ですが、新しいタイプの遺伝子治療で治し得る病気は、これからどんどん増えていくでしょうし、非常に良いタイミングでこのプロジェクトが始まったなと思っています。
横倉 ぜひ、すばらしい成果を上げて頂きたいと思います。
これからの医学教育の在り方とは
 横倉 先ほどの医学研究における臨床医の役割に関連してですが、「どうしても日々の臨床に追われて、なかなか余裕がない」という話を会員の先生方からよく聞くのですが、ちょっとした気付きから、いろいろな研究がスタートする訳ですよね。
横倉 先ほどの医学研究における臨床医の役割に関連してですが、「どうしても日々の臨床に追われて、なかなか余裕がない」という話を会員の先生方からよく聞くのですが、ちょっとした気付きから、いろいろな研究がスタートする訳ですよね。
末松 はい、全くおっしゃるとおりで、私自身は内科の臨床医から始めて9年ほど経って、留学を挟んで基礎研究の方に進んだのですが、難病の専門家でも何でもない訳です。
現在は専門医の資格を取るために必要不可欠な特定の基幹診療科の症例を集めて勉強する訳ですが、一度その専門分野が固まってしまうと、周辺の分野などにあまり目がいかなくなるという点があり、若い臨床医の先生方に対して期待と不安を感じています。
実は、このIRUDを我々の最初のリーディングプロジェクトとして選んだ理由の一つが、ここにあるのです。この領域は、特定の病気の専門家ではなかなか問題解決ができない病気ばかりで、非常に不思議なことに、一遺伝子の異常で起こる病気は、multiple system disordersといって、そのうちの30~40%には知的障害や発達障害など、何らかの神経系の異常が見つかることが多いのですが、骨格筋とか骨髄といった、神経以外の思わぬところに並行して出てくる異常もあります。そういうところに目配りとか気付きをどうやってもたらすかという意味で、非常に重要なプロジェクトなのです。専門医の認定を取ることだけに汲々として、"水平的思考"ができる医師が少なくなることは、国の医療の力を損なうことになる訳で、我々は意識して横串的なものをどんどん出していくべきと考えておりますし、若い先生方にはフィールドにこだわらず、"自分の可能性"を広げて欲しいと思います。
横倉 昔、私達が教育を受けた頃は、内科でも外科でも非常に幅広い診療を要求されたものですが、今では狭くなり過ぎて、専門外のことは「できません」「知りません」と言う先生が増えているようですので、これを少し幅広い診療領域から自分の専門性を確立するように改めていきたいですね。
末松 がんの研究も臓器別だったのが、最近では遺伝子解析が進み、特定のドライバー遺伝子の変異による増殖に対する特異的な阻害剤を投与すると、またドライバー遺伝子が変異して増殖をするようになるということで、臓器別ではなく、分子別な訳ですね。そういう意味で、消化器の専門、肺の専門だということではなく、がんを本当にコントロールするためには、全体として理解できるような若手の医師が育つように工夫してやっていかないと困るなと思っています。
横倉 先生は慶應義塾大学の医学部長として医学教育の改革にも取り組まれたそうですが、医学教育で変えた方がいいという点はございますか。
末松 在任中にやり切れなかったことでもあるのですが、今、申し上げた縱割りの診療科ですね。縱割りで深くやるのはもちろん結構なのですが、横串のプログラムが入っていないと、自分が医療全体の中でどの座標にいるのかが、若い人にはなかなか理解しにくくなると思うのです。そのために、臨床遺伝学とか、ファースト・イン・ヒューマン(first-in-human:医薬品の第Ⅰ相臨床試験において人間に初めて投与する試験)を系統的に教えるプログラムなど、いろいろな大学で取り組みが始められていますが、横串のプログラムが若いうちにどれくらいインプットされているかがとても重要だと思います。
それから、アメリカの強みは、病理学という、客観的な知見に基づいて医療の最後の診断をつける権限を持った人が、同時にゲノム研究をやっていることだと思います。日本の場合は、臨床病理をやっているゲノムのエキスパートの数が非常に少ないのです。がんの領域でゲノム医療を広げていこうという時に、一番ボトルネック(隘路(あいろ))になるのは、クリニカルパソロジー(clinical pathology:臨床病理)とモレキュラーバイオロジー(molecular biology:分子生物学)の両方を理解している人材が不足していることで、これは医学教育の責任であり、全医学部が協力して取り組むべきだと思います。
横倉 日本の医学生は本当に真面目で、道を示せばどんどん伸びるだろうと思うのですが。
末松 そう思います。医師の数も増えてきたと言われていますが、多様性を考えると、活躍の場はどこにでもあるのではないでしょうか。私は今、教育の仕組みに直接携わる立場ではありませんが、人材の不足が隘路になって良い医療を提供できていない分野がいくつかありますので、意見をきちんと出していきたいなと思っています。
横倉 会員の先生方にもその意義を理解してもらい、広めていきたいと考えております。本日は、ありがとうございました。
| 末松(すえまつ) 誠(まこと) 氏 国立研究開発法人日本医療研究開発機構理事長 1957年東京都生まれ。1983年慶應義塾大学医学部卒業。1988年同大助手。医学部内科学教室。1990年中央臨床検査部内視鏡部門。1990年第14回ヨーロッパ微小循環学会Young Investigator's Award受賞。1991年慶大医学部内科学教室帰室。直後にカリフォルニア大学サンディエゴ校応用生体医工学部留学。2001年慶大教授(医化学教室)を経て、2007年同大医学部長。 2015年国立研究開発法人日本医療研究開発機構初代理事長就任。 |



